Treonina
| Formula strutturale | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
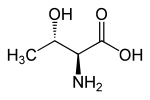
| Formula strutturale di L- treonina, l'isomero naturale | ||||||||||||||||||||||
| Generale | ||||||||||||||||||||||
| Cognome | Treonina | |||||||||||||||||||||
| altri nomi |
|
|||||||||||||||||||||
| Formula molecolare | C 4 H 9 NO 3 | |||||||||||||||||||||
| Breve descrizione |
solido incolore con un odore caratteristico |
|||||||||||||||||||||
| Identificatori / database esterni | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Informazioni sui farmaci | ||||||||||||||||||||||
| Codice ATC | ||||||||||||||||||||||
| proprietà | ||||||||||||||||||||||
| Massa molare | 119,12 g · mol -1 | |||||||||||||||||||||
| Stato fisico |
fermamente |
|||||||||||||||||||||
| Punto di fusione |
255 ° C ( decomposizione , L- treonina) |
|||||||||||||||||||||
| pK s valore |
|
|||||||||||||||||||||
| solubilità |
|
|||||||||||||||||||||
| istruzioni di sicurezza | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Dati tossicologici | ||||||||||||||||||||||
| Per quanto possibile e consuetudine, vengono utilizzate le unità SI . Salvo diversa indicazione, i dati forniti si applicano a condizioni standard . | ||||||||||||||||||||||
La treonina , abbreviata Thr o T , è un α - amminoacido proteinogenico essenziale nella sua forma L naturale .
Nella treonina c'è un gruppo idrossile sull'atomo di β-carbonio (= 3 posizioni) ; può anche essere visto come 3-metil- serina o 3-idrossilato desmetil valina . A causa del gruppo idrossile, la treonina è molto più polare e reattiva della valina.
La treonina è uno degli amminoacidi polari. Può essere fosforilato sul suo gruppo idrossile, che può svolgere un ruolo nella regolazione degli enzimi.
Stereochimica
La treonina ha due centri stereogenici sugli atomi di carbonio nella posizione 2 e 3. Esistono quindi quattro stereoisomeri di treonina con le seguenti configurazioni assolute: (2 S , 3 R ), (2 R , 3 S ), (2 S , 3 S ) e (2 R , 3 R ). Le proteine legate contenute nella L treonina hanno una configurazione (2 S , 3 R ) e sono fornite anche (2 S , 3 R acido ammino-3-idrossi-butanoico, -2 (designazione secondo la) IUPAC - Nomenclatura ) citata. Gli altri tre stereoisomeri [(2 R , 3 S ) -treonina, (2 S , 3 S ) -allo- treonina e (2 R , 3 R ) -allo- treonina] di L- treonina sono di poca importanza.
Quando si parla di "treonina" senza alcun nome aggiuntivo ( prefisso ), si parla comunemente di L- treonina .
| Isomeri di treonina | ||||
| Cognome | L- Treonina | D- Treonina | L - allo- treonina | D - allo- treonina |
| altri nomi | Acido (2 S , 3 R ) -2-ammino-3-idrossibutanoico | Acido (2 R , 3 S ) -2-ammino-3-idrossibutanoico | (2 S , 3 S ) - acido allo -2-ammino-3-idrossibutanoico | (2 R , 3 R ) - acido allo -2-ammino-3-idrossibutanoico |
| Formula strutturale |  |
 |
 |

|
| numero CAS | 72-19-5 | 632-20-2 | 28954-12-3 | 24830-94-2 |
| 80-68-2 (non specificata) | ||||
| Numero CE | 200-774-1 | 211-171-8 | 249-327-2 | 246-488-0 |
| 201-300-6 (non specificato) | ||||
| Scheda informativa ECHA | 100.000.704 | 100.010.157 | 100.044.829 | 100.042.247 |
| 100.001.183 (non spec.) | ||||
| PubChem | 6288 | 69435 | 99289 | 90624 |
| 205 (non specifica) | ||||
| DrugBank | DB00156 | DB03700 | - | - |
| - (non specificato) | ||||
| Numero FL | 17.021 (non specific.) | |||
| Wikidata | Q186521 | Q44073885 | Q27103859 | Q27094610 |
| Q60662943 (non specific.) | ||||
Evento
La treonina è un componente delle proteine animali e vegetali . Si presume che il fabbisogno giornaliero per gli adulti sia di circa 16 mg per kg di peso corporeo. I seguenti esempi per il contenuto di treonina si riferiscono ciascuno a 100 g di alimento; viene fornita anche la percentuale di proteine totali.
| Cibo | proteina | Treonina | proporzione di |
|---|---|---|---|
| Manzo, crudo | 21,26 g | 849 mg | 4,0% |
| Filetto di petto di pollo, crudo | 23,09 g | 975 mg | 4,2% |
| Salmone, crudo | 20,42 g | 860 mg | 4,2% |
| Uovo di pollo | 12,58 g | 556 mg | 4.4% |
| Latte vaccino, 3,7% di grassi | 3,28 g | 148 mg | 4,5% |
| Noci | 15,23 g | 596 mg | 3,9% |
| Farina integrale | 13,70 g | 395 mg | 2,9% |
| Farina di mais integrale | 6,93 g | 261 mg | 3,8% |
| Riso, non sbucciato | 7,94 g | 291 mg | 3,7% |
| Piselli secchi | 24,55 g | 872 mg | 3,6% |
Tutti questi alimenti contengono L- treonina legata chimicamente come componente proteico, solo in casi eccezionali L- treonina libera . Nel pesce le proteine antigelo sono costituite quasi esclusivamente da L- treonina e L- alanina .
storia
Il biochimico americano William Cumming Rose ha affrontato intensamente l'importanza degli amminoacidi per la nutrizione durante la sua carriera scientifica. Negli esperimenti sui ratti negli anni '30, scoprì che l'alimentazione dei 19 amminoacidi noti fino a quel momento non era sufficiente per la crescita dei ratti. Ha quindi cercato sistematicamente un altro amminoacido essenziale; finalmente è stato in grado di isolarli dalla fibrina e identificarli secondo la loro struttura. Con questo amminoacido noto come treonina, è stato scoperto l'ultimo degli amminoacidi proteinogenici canonici . Il nome treonina è stato scelto a causa della struttura a tre basi di questo amminoacido.
proprietà
I dati qui riportati si riferiscono solo alla L- treonina e alla D- treonina.
- Nome residuo: treonile
- Catena laterale : idrofila
- punto isoelettrico : 5.64
- Volume di Van der Waals : 93
- Liposolubilità : log K OW = −0,7
biosintesi
Poiché la L- treonina è uno degli amminoacidi essenziali, la L- treonina deve essere assunta con la dieta attraverso proteine contenenti L- treonina. Nelle piante e nei microrganismi, la biosintesi della L- treonina inizia da L - aspartato , le cui origini ( ossalacetato ) provengono dal ciclo del citrato . La L -aspartato avviene attraverso due stadi intermedi, per mezzo di enzimi corrispondenti (aspartato chinasi, aspartato semialdeide deidrogenasi, omoserina deidrogenasi) per L - omoserina implementata. In una fase successiva, l'alcool primario viene fosforilato dalla L- omoserina da una chinasi omoserina. Nell'ultimo passaggio, questa fosfoomoserina viene convertita dall'omoserina fosfato mutafosfatasi (PLP) in L- treonina .
Smantellamento
Per la ripartizione, comprese le formule strutturali, vedere la sezione Collegamenti Web
La L treonina è ridotta ad acetaldeide e glicina , che è della treonina aldolasi ( EC 4.1.2.5 catalizzata). L'amminoacido può anche essere convertito in propionil-CoA .
Produzione
La L- treonina può essere ottenuta da idrolizzati proteici utilizzando il metodo di estrazione con l'ausilio di scambiatori di ioni . Oggi, tuttavia , la L- treonina viene prodotta principalmente per fermentazione .
uso
Come componente delle soluzioni per infusione di amminoacidi [Aminoplasmal ® (D), Aminosteril ® -N-Hepa (D), Primene ® (A)] per la nutrizione parenterale, la L- treonina, insieme ad altri amminoacidi, è ampiamente utilizzata nell'uomo medicinale. Una “dieta chimicamente definita” somministrata per via orale contenente L- treonina è stata sviluppata per pazienti con disturbi digestivi . In questa dieta, gli amminoacidi sono la fonte dell'azoto; tutti i nutrienti vitali sono in una forma chimicamente definita con precisione.
Molti tipi di cereali hanno un contenuto di aminoacidi essenziali troppo basso. In conseguenza di questa mancanza di un solo amminoacido, la fruibilità di tutti gli amminoacidi ingeriti scende al valore determinato dall'amminoacido essenziale (“amminoacido limitante”) contenuto in quantità troppo piccola. Il valore nutritivo del cereale viene poi incrementato dall'aggiunta mirata di piccole quantità di quegli amminoacidi essenziali che ne sono carenti. Ad eccezione del mais, la maggior parte dei cereali contiene meno L- treonina di quanto richiesto dal bestiame. L'aggiunta di L- treonina ai mangimi composti è molto diffusa nell'industria dei mangimi e quindi preserva le risorse naturali.
link internet
Prove individuali
- ↑ Voce su THREONINE nel database CosIng della Commissione UE, accesso 28 dicembre 2020.
- ↑ a b c scheda tecnica treonina (PDF) di Merck , accesso 25 dicembre 2019.
- ↑ a b Scheda tecnica L-Threonine, 98 +% da AlfaAesar, consultato il 25 dicembre 2019 ( PDF )(JavaScript richiesto) .
- ^ A b c Carl S. Vestling, Donald T. Warner: I punti isoelettrici della treonina e di alcuni composti correlati . In: Journal of Biological Chemistry . nastro 144 , n. 3 , 1942, pagg. 687–690 (inglese, jbc.org [PDF]).
- ↑ Voce sulla L-treonina. In: Römpp Online . Georg Thieme Verlag, consultato il 30 maggio 2014.
- ↑ Scheda dati di Threonine da Sigma-Aldrich , consultata il 17 ottobre 2016 ( PDF ).
- ↑ DH Baker: tolleranza per gli amminoacidi a catena ramificata negli animali da esperimento e nell'uomo , in: J. Nutr. , 2005 , 135 (6) , pagg. 1585S-1590S; PMID 15930474 .
- ^ Database dei nutrienti del dipartimento dell'agricoltura, ventunesima edizione.
- ^ GC Barrett: Chimica e biochimica degli amminoacidi , Chapman and Hall, Londra, New York, 1985, p. 11, ISBN 0-412-23410-6 .
- ↑ S. Hansen: La scoperta degli amminoacidi proteinogenici dal 1805 a Parigi al 1935 nell'Illinois. ( Memento del 15 giugno 2016 in Internet Archive ) Berlino 2015.
- ↑ WC Rose, Esperimenti di alimentazione con miscele di amminoacidi altamente purificati: I. L'inadeguatezza delle diete contenenti diciannove amminoacidi , J Biol Chem, Volume 94, p. 155ss (1931)
- ↑ WC Rose, RH McCoy e CE Meyer, Esperimenti di alimentazione con miscele di amminoacidi altamente purificati: VIII. Isolamento e identificazione di un nuovo amminoacido essenziale , J Biol Chem, Volume 112, pp. 283ff. (1935).
- ↑ Bernd Hoppe e Jürgen Martens: Amino Acids - Production and Production , in: Chemistry in our time , 1984 , 18 , pp. 73–86; doi: 10.1002 / ciuz.19840180302 .
- ↑ a b Yoshiharu Izumi, Ichiro Chibata, Tamio Itoh: Production and Use of Amino Acids , in: Angewandte Chemie (journal) , 1978, 90 (3), pp. 187-194; doi: 10.1002 / anie.19780900307 .
