Acido fumarico
| Formula strutturale | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
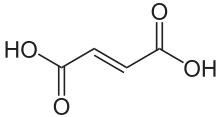
| |||||||||||||||||||
| Generale | |||||||||||||||||||
| Cognome | Acido fumarico | ||||||||||||||||||
| altri nomi | |||||||||||||||||||
| Formula molecolare | C 4 H 4 O 4 | ||||||||||||||||||
| Breve descrizione |
cristalli incolori e inodori |
||||||||||||||||||
| Identificatori / database esterni | |||||||||||||||||||
| |||||||||||||||||||
| Informazioni sui farmaci | |||||||||||||||||||
| Codice ATC | |||||||||||||||||||
| proprietà | |||||||||||||||||||
| Massa molare | 116,07 g mol −1 | ||||||||||||||||||
| Stato fisico |
fermamente |
||||||||||||||||||
| densità |
1,64 g cm −3 (20 ° C) |
||||||||||||||||||
| Punto di fusione |
287 ° C (capillare chiuso) |
||||||||||||||||||
| Punto di sublimazione |
200 ° C |
||||||||||||||||||
| Pressione del vapore |
<0,1 Pa (20 ° C) |
||||||||||||||||||
| pK s valore |
|
||||||||||||||||||
| solubilità |
povero di acqua (4,9 g l −1 a 20 ° C) |
||||||||||||||||||
| istruzioni di sicurezza | |||||||||||||||||||
| |||||||||||||||||||
| Dati tossicologici | |||||||||||||||||||
| Proprietà termodinamiche | |||||||||||||||||||
| ΔH f 0 |
−811,7 kJ / mol |
||||||||||||||||||
| Per quanto possibile e consuetudine, vengono utilizzate le unità SI . Salvo diversa indicazione, i dati forniti si applicano a condizioni standard . | |||||||||||||||||||
L'acido fumarico è il nome comune di una sostanza chimica organica presente in natura. Si tratta di un insaturo acido dicarbossilico con l'IUPAC nome trans acido -butenedioic , chiamato anche trans dicarbossilico -etilene acido. I loro sali sono chiamati fumarati . La forma cis isomerica è chiamata acido maleico .
storia
Nel 1937 Albert Szent-Györgyi ricevette il Premio Nobel per la medicina per il suo lavoro biochimico, compreso l'acido fumarico.
Presenza e produzione
L'acido fumarico si trova in grandi quantità in varie piante, funghi e licheni. Prende il nome dal fumo di terra comune (Fumaria officinalis) , che contiene grandi quantità di acido.
Fumarico acido è prodotta sinteticamente da maleico acido mediante isomerizzazione . Questo viene fatto riscaldando a oltre 150 ° C, mediante radiazione UV o cataliticamente in una soluzione acquosa.
Si manifesta in tutti gli organismi (ad esempio in diversi generi di Mucorales ) su diverse vie metaboliche biochimiche:
- come intermedio nella citrico acido ciclo attraverso l'ossidazione di acido succinico in presenza dell'enzima succinato deidrogenasi ( un'ossidoriduttasi )
- nel ciclo dell'urea scindendo l'acido succinico arginina
- nella biosintesi dei nucleotidi purinici ( dall'aspartato )
- nel metabolismo nucleotidico nella rappresentazione dell'adenosina monofosfato da inosina monofosfato
- attraverso la scomposizione idrolitica di amminoacidi come fenilalanina e tirosina
- da deaminazione di acido aspartico
proprietà
L'acido fumarico non ha un punto di fusione a pressione normale, ma sublima da circa 200 ° C. A temperatura ambiente forma cristalli bianchi, quasi inodori, infiammabili. La soluzione acquosa è fortemente acida: 1 litro di acqua con 4,9 g di acido fumarico disciolto ha un valore di pH di 2,1. L'acido biprotonico ha un pK s 1 di 3.0 e un pK s 2 di 4.5. Il composto si dissolve solo leggermente in acqua. A 15,5 ° C, solo 0,428 g di acido fumarico si sciolgono in 100 g di acqua; a 100 ° C. la solubilità sale a 9,97 g per 100 g di acqua. Il punto di infiammabilità dell'acido fumarico è 273 ° C, la temperatura di decomposizione è> 350 ° C e la temperatura di accensione è 375 ° C.
uso
L'acido fumarico è approvato come additivo alimentare E 297 ed è usato come acidificante . Nella chimica sintetica viene utilizzato per la produzione di poliestere . Nella biotecnologia, l'ammoniaca è attaccata stereoselettivamente al doppio legame carbonio-carbonio, si forma acido L - aspartico catalizzato da enzimi . Molti di vista farmaceutico sostanze attive - in particolare quelli contenenti amminoacidi gruppi - vengono somministrati come sali dell'acido fumarico. Gli esteri dell'acido fumarico come il dimetilfumarato e il monoetilfumarato sono usati per trattare la psoriasi e, da marzo 2013, la sclerosi multipla recidivante-remittente .
Nell'allevamento dei suini, l'acido fumarico viene utilizzato come additivo alimentare per i suinetti per prevenire le infezioni correlate al coli mantenendo il valore del pH nell'intestino sufficientemente basso.
È stato dimostrato che l'acido fumarico come additivo per mangimi negli agnelli può ridurre la loro produzione di metano fino al 70%.
L'acido fumarico è utilizzato anche nei prodotti cosmetici . Viene utilizzato come sostanza tampone e stabilizza il valore del pH del cosmetico.
link internet
Prove individuali
- ↑ Voce sull'ACIDO FUMARICO nel database CosIng della Commissione UE, accesso 28 dicembre 2019.
- ↑ Voce su E 297: acido fumarico nel database europeo degli additivi alimentari, accesso 6 agosto 2020.
- ↑ un b c d e f g h i j k l inserimento in acido fumarico nella banca dati delle sostanze GESTIS del l' IFA , letta il 16 dicembre, il 2019. (JavaScript richiesto)
- ↑ a b c A. Reichert: Titolazioni potenziometriche in teoria e pratica. ( Memento del 1 aprile 2007 in Internet Archive )
- ↑ a b chem.wisc.edu: pKa Data , Compilato da R. Williams (PDF, 78 kB).
- ↑ L'iscrizione dell'acido fumarico nel inventario classificazione ed etichettatura delle della Agenzia europea delle sostanze chimiche (ECHA), accede il 1 ° febbraio, 2016. I produttori o distributori possono ampliare la classificazione e l'etichettatura armonizzate .
- ↑ David R. Lide (a cura di): Manuale CRC di chimica e fisica . 90a edizione. (Versione Internet: 2010), CRC Press / Taylor e Francis, Boca Raton, FL, Proprietà termodinamiche standard delle sostanze chimiche, pagg. 5-25.
- ↑ K. Lohbeck, H. Haferkorn, W. Fuhrmann, N. Fedke: Maleic and Fumaric Acids. In: Enciclopedia della chimica industriale di Ullmann. Wiley-VCH Verlag, Weinheim 2012. doi : 10.1002 / 14356007.a16_053 .
- ↑ Società tedesca per la sclerosi multipla: semaforo verde per acido fumarico e teriflunomide per il trattamento della sclerosi multipla recidivante. ( Memento del 25 maggio 2013 in Internet Archive ) 23 marzo 2013.
- ↑ Scienziati cercano di tagliare la flatulenza della mucca m.phys.org, 21 marzo 2008, accesso 30 novembre 2019
- ↑ Marina Bährle-Rapp: Aleurites moluccana . In: Springer Lexicon Cosmetics and Body Care . 4a edizione. Springer, 2012, ISBN 978-3-642-24688-3 , pagg. 221 ( anteprima limitata nella ricerca di Google Libri).


