Carbammato di ammonio
| Formula strutturale | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
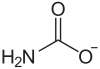 
| |||||||||||||||||||
| Generale | |||||||||||||||||||
| Cognome | Carbammato di ammonio | ||||||||||||||||||
| altri nomi |
|
||||||||||||||||||
| Formula molecolare | H 2 NCOONH 4 | ||||||||||||||||||
| Breve descrizione |
solido bianco con un odore simile all'ammoniaca |
||||||||||||||||||
| Identificatori / database esterni | |||||||||||||||||||
| |||||||||||||||||||
| proprietà | |||||||||||||||||||
| Massa molare | 78,07 g mol −1 | ||||||||||||||||||
| Stato fisico |
fermamente |
||||||||||||||||||
| densità |
1,6 g cm −3 |
||||||||||||||||||
| Punto di fusione |
152 ° C (in fiala chiusa) |
||||||||||||||||||
| punto di ebollizione |
Decomposizione da 35 ° C |
||||||||||||||||||
| Pressione del vapore |
117,70 h Pa (25 ° C) (decomposizione) |
||||||||||||||||||
| solubilità |
buono in acqua (790 g l −1 a 20 ° C) |
||||||||||||||||||
| istruzioni di sicurezza | |||||||||||||||||||
| |||||||||||||||||||
| Per quanto possibile e consuetudine, vengono utilizzate le unità SI . Salvo diversa indicazione, i dati forniti si applicano a condizioni standard . | |||||||||||||||||||
Il carbammato di ammonio , precedentemente chiamato anche carbammato di ammonio , è il sale di ammonio dell'acido carbammico , che non è noto allo stato libero. È un ingrediente minore nel sale staghorn .
proprietà
Il carbammato di ammonio forma una polvere cristallina incolore che si dissolve bene in acqua (a 790 g / l). La solubilità viene aumentata aggiungendo gas di ammoniaca . In soluzione acquosa, il carbammato di ammonio si idrolizza parzialmente sopra i 35 ° C e completamente sopra i 60 ° C, con la formazione di carbonato di ammonio , che a sua volta può decomporsi in ammoniaca e anidride carbonica .
Il decadimento può essere quantificato tramite le corrispondenti pressioni di dissociazione.
| Pressione di dissociazione del carbammato di ammonio | ||||||||||||
| temperatura | in ° C | 10.03 | 14.92 | 17.86 | 21.25 | 24.91 | 26.77 | 30.91 | 35.91 | 39.89 | 44.86 | |
| Stampa | in kPa | 3.89 | 5.66 | 7.03 | 9.08 | 11.77 | 13.37 | 17.85 | 24.89 | 32.33 | 44.21 | |
Quando riscaldato in un sistema chiuso, si può osservare la decomposizione in urea e acqua a temperature intorno alla temperatura ambiente . La velocità di conversione aumenta bruscamente con l'aumentare della temperatura, con l' acqua formata che ha un effetto catalitico.
sintesi
Il carbammato di ammonio è prodotto dalla reazione diretta del gas di ammoniaca e della CO 2 in un rapporto in volume di 2: 1 con l'esclusione dell'acqua .
uso
Il carbammato di ammonio è utilizzato nell'industria cosmetica e nella produzione di pesticidi. È anche un importante intermedio nella produzione di urea . Viene anche usato come agente pulente, decapante e neutralizzante, nonché nel sale di corno di cervo sopra menzionato per la cottura. In Germania, la produzione diretta di carbammato di ammonio è solo di circa 1000 t / a a causa della bassa domanda. L' industria automobilistica sta studiando il carbammato di ammonio come alternativa alla soluzione di urea AUS 32 nei convertitori catalitici SCR .
Prove individuali
- ↑ Voce su CARBAMMATO DI AMMONIO nel database CosIng della Commissione UE, accesso 28 dicembre 2020.
- ↑ un b c d e f g L'iscrizione carbammato di ammonio nella banca dati delle sostanze GESTIS del l' IFA , si accede il 1 febbraio 2016. (JavaScript richiesto)
- ↑ K.-H. Zapp, K.-H. Wostbrock, M. Schäfer, K. Sato, H. Seiter, W. Zwick, R. Creutziger, H. Head: Ammonium Componds. In: Enciclopedia della chimica industriale di Ullmann . Wiley-VCH Verlag, Weinheim 2005, doi : 10.1002 / 14356007.a02_243 .
- ↑ a b c T. R. Briggs, V. Migrdishian: The Amoniumn Carbamate Equilibrium. In: J. Phys. Chem. 28, 1923, pp 1121-1135,. Doi: 10.1021 / j150245a001 .






