Acido salicilico
| Formula strutturale | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
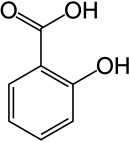
| ||||||||||||||||||||||
| Generale | ||||||||||||||||||||||
| Cognome | Acido salicilico | |||||||||||||||||||||
| altri nomi | ||||||||||||||||||||||
| Formula molecolare | C 7 H 6 O 3 | |||||||||||||||||||||
| Breve descrizione |
cristalli incolori e inodori, graffianti, dal sapore agrodolce con un retrogusto sgradevole |
|||||||||||||||||||||
| Identificatori esterni / banche dati | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Informazioni sui farmaci | ||||||||||||||||||||||
| Codice ATC | ||||||||||||||||||||||
| proprietà | ||||||||||||||||||||||
| Massa molare | 138,12 g mol −1 | |||||||||||||||||||||
| Stato fisico |
fermamente |
|||||||||||||||||||||
| densità |
1,44 gcm -3 |
|||||||||||||||||||||
| Punto di fusione |
159 °C |
|||||||||||||||||||||
| punto di ebollizione |
211°C ( 27hPa ) |
|||||||||||||||||||||
| p K S valore |
|
|||||||||||||||||||||
| solubilità |
|
|||||||||||||||||||||
| istruzioni di sicurezza | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Dati tossicologici |
|
|||||||||||||||||||||
| Per quanto possibile e consueto, vengono utilizzate unità SI . Salvo diversa indicazione, i dati forniti si applicano alle condizioni standard . | ||||||||||||||||||||||
L'acido salicilico ( o- idrossibenzoico acido ) è una sostanza chimica con antipiretiche ed analgesiche effetti. L'acido salicilico si trova sotto forma di suo estere metilico negli oli essenziali e come ormone vegetale nelle foglie , nei fiori e nelle radici di varie piante ed è importante per la difesa della pianta contro gli agenti patogeni . Ha preso il nome perché veniva ottenuto principalmente attraverso il processo ossidativo della salicina , che è contenuta nella corteccia di vari salici (scientificamente Salix spec. ).
È anche conosciuto con il nome di acido spirico , in quanto si può ottenere dal succo del cespuglio di passero ( olmaria ). Dal nome Spirsäure anche il nome del marchio deriva aspirina per l'acido acetilsalicilico da: A cetilico spir acido. I sali dell'acido salicilico sono chiamati salicilati .
Raffaele Piria isolò per primo l'acido salicilico dalla salicina (1838).
Presenza ed estrazione
biosintesi
L'acido salicilico si trova in un gran numero di piante e agisce come un fitoormone . Esistono due vie compartimentate di biosintesi: la via fenilpropanoide nel citoplasma a partire dalla fenilalanina e la via isocoresmata nei cloroplasti. La maggior parte dell'acido salicilico è metilato come salicilato di metile liquido per essere efficace come derivato volatile per il trasporto a lunga distanza. Nelle piante di tabacco e Arabidopsis thaliana è stato dimostrato che questa forma è importante per la resistenza acquisita sistemicamente. Inoltre, l'acido salicilico può essere glicosilato e immagazzinato nei vacuoli come forma inattiva.
Produzione tecnica
Tecnicamente, è prodotto da anidride carbonica e fenolato di sodio usando la reazione di Kolbe-Schmitt (indicata anche semplicemente come sintesi dell'acido salicilico) . Questa produzione artificiale ha ampiamente sostituito l'estrazione dalla corteccia di salice.
Già nel 1874, sulla base di un'idea di Hermann Kolbe , la sintesi dell'acido salicilico fu trasferita dal laboratorio alla produzione in fabbrica, con lo studente di Schmitt Friedrich von Heyden che dirigeva la fabbrica di acido salicilico Dr. F. von Heyden a Dresda, che si trasferì a Radebeul un anno dopo . Da lì, l'acido salicilico è stato venduto come il primo farmaco prodotto industrialmente e "confezionato" nel mondo. Friedrich von Heyden è considerato il fondatore della produzione industriale di acido salicilico nell'industria farmaceutica.
Proprietà chimico-fisiche
L'acido salicilico è uno degli aromatici a causa dell'anello benzenico che contiene . Poiché contiene un gruppo carbossilico e un gruppo ossidrile , appartiene agli acidi idrossicarbossilici . A causa della -stabilità del carbossi al gruppo ossidrile, può anche essere indicato come acido β-idrossicarbossilico. Poiché il gruppo ossidrile è legato direttamente all'anello benzenico aromatico, appartiene anche ai fenoli e quindi anche agli acidi fenolici .
Quando riscaldato rapidamente e vigorosamente, l'acido salicilico si decarbossila per formare fenolo . Al di sopra dei 76°C, la sostanza sublima parzialmente e dai vapori di raffreddamento si formano cristalli aghiformi .
L' elevata acidità - rispetto ad altri acidi idrossibenzoici - è dovuta alla stabilizzazione dell'anione salicilato attraverso un legame idrogeno con il vicino gruppo idrossile.
Prove analitiche: poiché l'acido salicilico è formalmente l' enolo (in questo caso un fenolo ) di un acido β-chetocarbossilico, forma un complesso di colore viola con una soluzione di cloruro di ferro (III) , il complesso di ferro tris-salicilato (III):
Questa evidenza non è specifica in quanto composti simili agli esteri acetoacetici hanno la stessa reazione. Il punto di infiammabilità è di 157°C e la temperatura di accensione è di 570°C.
Funzione biologica
Come fitormone, l'acido salicilico svolge un ruolo importante come segnale di regolazione negli stress abiotici come secchezza e calore, freddo o pressione osmotica. Inoltre, è importante per la pianta nella difesa dai patogeni, si esprime sia a livello locale che sistemico in caso di attacco ed è in grado di modulare l'espressione genica. Ci sono anche prove che l'acido salicilico svolge un ruolo nella crescita e nello sviluppo della pianta.
uso
L'acido salicilico viene utilizzato nella produzione di coloranti e fragranze e l'acido acetilsalicilico (ASA, noto anche con il marchio Aspirin ), che viene utilizzato come farmaco antidolorifico, antinfiammatorio e anticoagulante . Sotto forma di sale insolubile subsalicilato di bismuto , viene utilizzato contro la diarrea e i disturbi del tratto gastrointestinale.
L'acido salicilico è anche usato come fondente nella saldatura dolce .
L'acido salicilico ha un effetto antimicrobico , ma il suo uso come conservante negli alimenti è vietato. In cosmesi, l'acido salicilico è consentito ai sensi del Regolamento (CE) n. 1223/2009 sugli agenti cosmetici come agente antiforfora negli agenti di lavaggio dei capelli fino a un massimo del 3%, per altri agenti fino a una concentrazione del 2% e se utilizzato come conservante fino ad un massimo dello 0,5%. Nei medicinali , l'acido salicilico da una soluzione al 5% mostra un effetto cherato -e quindi anche comedolitico , sufficiente per la terapia dell'acne . In una soluzione al 10%, è usato per trattare calli , verruche e funghi della pelle .
effetti indesiderati
Effetti collaterali della farmacoterapia
L'acido salicilico è un metabolita dell'acido acetilsalicilico, che viene rapidamente idrolizzato nel corpo . Gli effetti collaterali sono principalmente reazioni allergiche , tendenza al sanguinamento, broncocostrizione ( asma bronchiale ), danno della mucosa gastrica con sanguinamento, in singoli casi danno epatico. Sono stati inoltre osservati ritenzione di acido urico, iperuricemia e danno renale. Un'importante via metabolica nel fegato è la conversione in acido salicilurico .
tossicità
Sulla pelle, sulle mucose e sugli occhi, l'acido salicilico è fortemente irritante per i danni ai tessuti. Inoltre, se assunto per via orale o meno, l'acido provoca uno smorzamento del centro respiratorio e un'interruzione di importanti processi metabolici e del sistema nervoso centrale . Con l'esposizione cronica, diventano evidenti i disturbi del tratto gastrointestinale. Negli esperimenti sugli animali, la somministrazione orale e cutanea di acido salicilico ha mostrato vari effetti sugli animali (gatti, topi, conigli e ratti) come sonnolenza, debolezza muscolare e danni agli organi del fegato e dei reni. La tossicità acuta DL 50 era compreso tra 400 e 1300 mg / kg per via orale e 2 g / kg dermica nei ratti. Nell'uomo, dopo somministrazione dermica sono stati determinati valori di TD Lo da 57 a 111 mg/kg. L' emivita plasmatica dell'acido salicilico è di circa 2-3 ore.
istruzioni di sicurezza
Su suggerimento di Novacyl, la classificazione chimica dell'acido salicilico è stata rivista nel 2015 e nel 2016. Il 10 marzo 2016 il Comitato per la valutazione dei rischi (RAC) dell'Agenzia europea per le sostanze chimiche (ECHA) ha modificato la classificazione dell'acido salicilico come segue: l'acido salicilico è classificato come tossico per la riproduzione Repr 2, nonché Acut Tox 4 e Eye Dam 1. Gli avvisi sono stati impostati su H361d, H302 e H318. Questa classificazione del RAC deve ancora essere recepita dalla Commissione UE nella normativa applicabile, ma con la pubblicazione rappresenta lo stato di conoscenza che deve essere preso in considerazione da aziende e autorità.
Derivati dell'acido salicilico
Sali
L'acido salicilico reagisce con la soda caustica per formare salicilato di sodio .
Estere
Se l'acido salicilico reagisce con un alcol , si forma un estere dell'acido carbossilico o un estere dell'acido salicilico con l'eliminazione dell'acqua . Può anche formare esteri con acidi organici , nel qual caso funziona quindi come un alcol nella reazione. Gli esteri dell'acido salicilico sono utilizzati principalmente nell'industria cosmetica e dei profumi come agenti antireumatici negli additivi per il bagno, unguenti o creme, nonché fragranze e filtri UV nelle creme solari. L'estere più noto dell'acido salicilico è l'acido acetilsalicilico . Qui il gruppo ossidrile di salicilico acido è stato esterificato con il gruppo carbossilico di acetico acido. Altri importanti esteri dell'acido salicilico sono metil salicilato , etil salicilato , benzil salicilato , isobutil salicilato , isopentil salicilato , fenil salicilato e idrossietil salicilato .
Derivati alogeni
Per bromurazione con bromo elementare in acido acetico glaciale , si forma acido 3,5-dibromosalicilico , il cui sale di rame viene utilizzato come fungicida e battericida .
L' acido 3,5-diiodosalicilico, di rilevanza biochimica , si ottiene per iodurazione con cloruro di iodio . I derivati dell'acido salicilico alogenati in posizione 4, come l'acido 4-iodosalicilico , non possono essere ottenuti direttamente.
letteratura
- F. von Heyden: Acido salicilico . In: Il gazebo . Numero 10, 1863, pp. 172 ( testo completo [ Wikisource ]).
- Il manuale di Beilstein . Volume 10, Textarchiv - Internet Archive (sull'acido salicilico e suoi derivati, letteratura registrata fino al 1910).
link internet
Evidenze individuali
- ↑ Inserimento su ACIDO SALICILICO nel database CosIng della Commissione UE, consultato il 14 gennaio 2020.
- ↑ L'iscrizione acido salicilico. In: Römpp Online . Georg Thieme Verlag, consultato il 1 giugno 2014.
- ↑ un b c d e f g h i Entrata in acido salicilico nella banca dati delle sostanze GESTIS del l' IFA , si accede il 14 gennaio 2020. (JavaScript richiesto)
- ↑ a b Manuale delle tabelle CRC per l'identificazione dei composti organici . Terza edizione, 1984, ISBN 0-8493-0303-6 .
- ↑ Claudia Synowietz, Klaus Schäfer (a cura di): Calendario chimico. 3. Edizione. Springer, Berlino/Heidelberg/New York/Tokyo 1984, ISBN 3-540-12652-X .
- ↑ L'iscrizione L'acido salicilico in inventario classificazione ed etichettatura delle della Agenzia europea delle sostanze chimiche (ECHA), accede il 30 dicembre 2019. I produttori o distributori possono ampliare la classificazione e l'etichettatura armonizzate .
- ↑ a b c Manuale di tossicologia. 4 volumi, WB Saunders Co., Filadelfia 1956-1959; Volume 5, 1959, pagina 148.
- ↑ a b Droga in Giappone. Volume 6, 1982, pagina 291.
- ↑ a b BIOFAX. Industrial Bio-Test Laboratories Inc., Schede tecniche. Volume 21-3 / 1971.
- ↑ a b Dati sulla tossicità acuta. Journal of the American College of Toxicology, Parte B. Volume 15 (Suppl.)
- ↑ a b P. A. Soyka, LF Soyka: Assorbimento di acido salicilico . In: Giornale dell'Associazione Medica Americana . nastro 244 , n. 7 , 1980, pp. 660-661 , PMID 7392165 (inglese, pmj.bmj.com [PDF]).
- ↑ a b C. M. Dwyer, RH McCloskey, RE Kerr: Avvelenamento da acido salicilico topico. In: Rivista medica post-laurea . nastro 70 , nr. 820 , 1994, pp. 146 , PMID 8170891 , PMC 2397637 (testo integrale libero).
- ^ Doris Schwarzmann-Schafhauser: acido salicilico. In: Werner E. Gerabek et al. (Ed.): Enciclopedia Medical History. De Gruyter, Berlino/New York 2005, ISBN 3-11-015714-4 , pagina 1282.
- ↑ Ad esempio Salix alba , Filipendula (Spirea) ulmaria e bacche di tè (Gautheria procumbens).
- ↑ a b M. Rivas-San Vicente, J. Plasencia: L'acido salicilico oltre la difesa: il suo ruolo nella crescita e nello sviluppo delle piante . In: Giornale di botanica sperimentale . nastro 62 , n. 10 , 1 giugno 2011, pag. 3321-3338 , doi : 10.1093/jxb/err031 .
- ↑ Specifica del brevetto (Brevetto tedesco DE4415527) sull'uso dell'acido salicilico o dell'acido acetilsalicilico nella saldatura dolce.
- ↑ AA Hartmann: L'influenza di vari fattori sulla flora cutanea residente nell'uomo . In: Seminari di Dermatologia . nastro 9 , n. 4 , 1990, pp. 305-308 , PMID 2285575 .
- ↑ Acido salicilico come conservante per articoli di consumo. Il loro valore, utilità e innocuità, giustificato dal giudizio di autorità competenti e conoscenza giudiziaria. Fabbrica chimica von Heyden, Radebeul-Dresden 1896 urn : nbn: de: hbz: 061: 2-11219 .
- ↑ Doris Fanta, Christine Messeritsch-Fanta: Acne 1999. Abbiamo ancora bisogno di un dermatologo? In: Il dermatologo . nastro 50 , nr. 12 dicembre 1999, pag. 900-911 , doi : 10.1007 / s001050051009 .
- ↑ AW Frahm, HHJ Hager, F. v. Bruchhausen, M. Albinus, H. Hager: Manuale di pratica farmaceutica di Hager: Volume 4: Sostanze AK. Birkhäuser, 1999, ISBN 978-3-540-52688-9 , pagina 42.
- ↑ Informazioni specialistiche Aspirin® 100 mg compresse ( Memento del 29 aprile 2006 in Internet Archive ; PDF).
- ^ Decisione del RAC del 10 marzo 2016
- ↑ Brevetto US 399034: Sali biocidi dell'acido 3,5-dibromosalicilico .








