Einsteinio
| proprietà | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| In genere | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nome , simbolo , numero atomico | Einsteinio, Es, 99 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria dell'elemento | attinidi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo , periodo , blocco | Ac , 7 , f | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| numero CAS | 7429-92-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomico | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa atomica | 252 e | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio atomico | 203 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurazione elettronica | [ Rn ] 5 f 11 7 s 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Energia di ionizzazione | 6°.36758 (25) eV ≈ 614.38 kJ / mole | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Energia di ionizzazione | 12°.2 (4) eV ≈ 1 180 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Energia di ionizzazione | 22.7 (4) eV ≈ 2 190 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Energia di ionizzazione | 38.8 (4) eV ≈ 3 740 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Energia di ionizzazione | 54.1 (1,9) eV ≈ 5 220 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fisicamente | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stato fisico | fermamente | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modifiche | 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struttura di cristallo | cubo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| densità | (calcolato) 8,84 g / cm 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di fusione | 1133 K (860 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto di ebollizione | 1269K (996°C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chimicamente | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stati di ossidazione | +2, +3 , (+4) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Potenziale normale | (Es 3+ + 3 e - → Es) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| isotopi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Per altri isotopi, vedere l' elenco degli isotopi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informazioni sui pericoli e sulla sicurezza | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Radioattivo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Per quanto possibile e consueto, vengono utilizzate unità SI . Salvo diversa indicazione, i dati forniti si applicano alle condizioni standard . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Einsteinio è un elemento chimico prodotto esclusivamente artificialmente con il simbolo dell'elemento Es e il numero atomico 99. Nella tavola periodica è nel gruppo degli attinidi ( 7° periodo , blocco f ) ed è uno degli elementi transuranici . L'einsteinio è un metallo radioattivo che può essere prodotto solo con grande sforzo in quantità quasi pesabili. Fu scoperto nel 1952 dopo il test della prima bomba all'idrogeno americana e chiamato così in onore di Albert Einstein , che però non aveva nulla a che fare con la scoperta o la ricerca dell'Einsteinio. Viene prodotto in quantità molto piccole nei reattori nucleari . Il metallo ei suoi composti sono ottenuti in piccole quantità principalmente per scopi di studio.
storia


L'einsteinio è stato trovato insieme al fermio dopo aver testato la prima bomba all'idrogeno americana, Ivy Mike , il 1 novembre 1952 sull'atollo di Eniwetok . I primi campioni sono stati ottenuti su carte da filtro che venivano trasportate durante il volo attraverso la nuvola di esplosione. Quantità maggiori sono state successivamente isolate dai coralli. Per motivi di segreto militare, i risultati non furono inizialmente pubblicati.
Una prima indagine sui resti dell'esplosione aveva mostrato la formazione di un nuovo isotopo di plutonio 244 Pu, che avrebbe potuto derivare solo dall'assorbimento di sei neutroni da parte di un nucleo di uranio- 238 e da due successivi decadimenti .
All'epoca si credeva che l'assorbimento di neutroni da parte di un nucleo pesante fosse un evento raro. Tuttavia, l'identificazione di 244 Pu ha suggerito che i nuclei di uranio possono catturare molti neutroni, dando luogo a nuovi elementi.
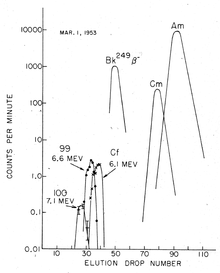
Gli ioni attinidi disciolti sono stati separati in presenza di un tampone acido citrico / citrato di ammonio in un mezzo debolmente acido ( pH ≈ 3,5) con scambiatori ionici a temperatura elevata. L'elemento 99 (Einsteinium) è stato rilevato rapidamente; l' isotopo 253 Es, un emettitore α ad alta energia (6,6 MeV), è stato scoperto per la prima volta. Viene creato catturando 15 neutroni da 238 U, seguiti da sette decadimenti β.
Questa formazione mediante cattura continua di neutroni era possibile perché al momento della detonazione la densità del flusso di neutroni era così alta che la maggior parte dei nuclei atomici - radioattivi - che si erano formati nel frattempo non erano ancora decaduti alla successiva cattura di neutroni. Nel caso di un flusso di neutroni molto elevato, il numero di massa aumenta bruscamente senza che il numero atomico cambi. Solo allora i nuclidi instabili risultanti decadono su molti decadimenti in nuclidi stabili o instabili con un numero atomico elevato:
Nel settembre 1953 non si sapeva quando sarebbero stati pubblicati i risultati delle squadre di Berkeley , Argonne e Los Alamos . Si decise di produrre i nuovi elementi attraverso esperimenti di bombardamento; Allo stesso tempo, è stato assicurato che questi risultati non sarebbero caduti nella segretezza e potrebbero quindi essere pubblicati. Gli isotopi di Einsteinio furono prodotti poco dopo al Radiation Laboratory dell'Università della California bombardando l'uranio ( 238 U) con azoto ( 14 N). È stato notato che esiste una ricerca su questo elemento che è stata finora tenuta segreta. Gli isotopi dei due elementi appena scoperti sono stati generati irradiando l'isotopo di plutonio 239 Pu, ei risultati sono stati pubblicati in cinque pubblicazioni in rapida successione. Le reazioni finali di Californium sono:
Il team di Berkeley era anche preoccupato che un altro gruppo di ricercatori potesse scoprire e pubblicare gli isotopi più leggeri dell'elemento 100 mediante bombardamento ionico prima di poter pubblicare la loro ricerca classificata. Perché alla fine del 1953 come all'inizio del 1954 un gruppo di lavoro dell'Istituto Nobel per la Fisica di Stoccolma sparò a nuclei di uranio con nuclei di ossigeno; si è formato l'isotopo con numero di massa 250 dell'elemento 100 ( 250 μm).
Il team di Berkeley ha già pubblicato alcuni risultati sulle proprietà chimiche di entrambi gli elementi. Infine, i risultati dell'esplosione termonucleare furono resi noti nel 1955 e poi pubblicati.
Alla fine, la priorità del team di Berkeley è stata universalmente riconosciuta, poiché le loro cinque pubblicazioni hanno preceduto la pubblicazione svedese e potevano fare affidamento sui risultati precedentemente segreti dell'esplosione termonucleare del 1952. Questo era associato al privilegio di nominare i nuovi elementi. Decisero di chiamarli come famosi scienziati deceduti. Si convenne subito di dare i nomi in onore di Albert Einstein ed Enrico Fermi , entrambi da poco scomparsi: “Suggeriamo per il nome dell'elemento con numero atomico 99, einsteinio (simbolo E) da Albert Einstein e per il nome per l'elemento con numero atomico 100, fermio (simbolo Fm), dal nome di Enrico Fermi. “L'annuncio per i due elementi appena scoperti Einsteinio e Fermio è stato fatto da Albert Ghiorso alla 1a Conferenza Atomica di Ginevra , che si è svolta dalle 8 al Si è svolta il 20 agosto 1955. Il simbolo dell'elemento per Einsteinium è stato successivamente cambiato da E a Es .
isotopi
Tutti i 17 nuclidi e i 3 isomeri nucleari conosciuti fino ad oggi sono radioattivi e instabili. I numeri di massa noti vanno da 241 a 258. L'isotopo 252 Es ha l'emivita più lunga con 471,7 giorni, quindi non possono esserci più eventi naturali sulla terra. 254 Ha un'emivita di 275,7 giorni, 255 Es di 39,8 giorni e 253 Es di 20,47 giorni. Tutti gli altri isotopi radioattivi hanno un'emivita inferiore a 40 ore e la maggior parte di essi è inferiore a 30 minuti. Dei 3 isomeri principali, 254 m Es è il più stabile con t ½ = 39,3 ore.
→ Elenco degli isotopi di Einsteinio
Estrazione e presentazione
L'einsteinio viene creato bombardando attinidi più leggeri con neutroni in un reattore nucleare. La fonte principale è il reattore isotopico ad alto flusso da 85 MW presso l' Oak Ridge National Laboratory nel Tennessee, USA, che è impostato per la produzione di elementi transcuriali (Z>96).
Nel 1961, è stato sintetizzato abbastanza einsteinio per produrre una quantità pesabile dell'isotopo 253 Es. Questo campione pesava circa 0,01 mg ed era usato per fare il Mendelevio . Un altro Einsteinio è stato prodotto all'Oak Ridge National Laboratory bombardando 239 Pu con neutroni . Sono stati ottenuti circa 3 milligrammi in quattro anni di irradiazione continua da un chilogrammo di plutonio e successiva separazione.
Estrazione degli isotopi di Einsteinio
Piccole quantità di einsteinio e fermio sono state isolate e separate dal plutonio , che è stato irradiato con neutroni. Sono stati trovati quattro isotopi di Einsteinio (con i dettagli delle emivite misurate all'epoca):
- 253 Es: emettitori α con t ½ = 20,03 giorni e con un'emivita di fissione spontanea di 7 × 10 5 anni
- 254 m Es: -emettitore con t ½ = 38,5 ore
- 254 Es: α emettitori con t ½ ≈ 320 giorni
- 255 Es: -emettitori con t ½ = 24 giorni
Sono stati trovati due isotopi di fermio:
- 254 Fm: emettitori α con t ½ = 3,24 ore e con un'emivita di fissione spontanea di 246 giorni
- 255 Fm: α-emettitore con t ½ = 21,5 ore
Bombardare l'uranio con atomi di azoto ionizzato cinque volte e atomi di ossigeno ionizzati sei volte ha prodotto anche isotopi di Einsteinio e Fermio.
L'isotopo 248 Es è stato identificato quando 249 Cf è stato bombardato con deuterio. Decade principalmente per cattura di elettroni (ε) con un'emivita di 25 ± 5 minuti ma anche per emissione di particelle α (6,87 ± 0,02 MeV). Il rapporto (ε/α) di ∼ 400 potrebbe essere identificato dalla quantità di 248 Cf generata dalla cattura elettronica .
Gli isotopi 249 Es, 250 Es, 251 Es e 252 Es sono stati generati bombardando 249 Bk con particelle α. Quindi 4 a 1 neutroni possono lasciare il nucleo, in modo che sia possibile la formazione di quattro diversi isotopi.
Sebbene l'isotopo 252 Es abbia l'emivita più lunga, l'isotopo 253 Es è più facilmente accessibile e viene utilizzato principalmente per determinare le proprietà chimiche. È stato ottenuto irradiando da 100 a 200 μg 252 Cf con neutroni termici (densità di flusso: da 2 a 5 × 10 14 neutroni × cm -2 s -1 , periodo di tempo: da 500 a 900 h). Per la separazione è stato utilizzato α-idrossiisobutirrato di ammonio .
Raffigurazione dell'Einsteinio elementare
L'Einsteinio si ottiene riducendo il fluoruro di Einsteinio (III) con litio o l'ossido di Einsteinio (III) con lantanio .
proprietà
Nella tavola periodica , l'Einsteino con numero atomico 99 è nella serie degli attinoidi, il suo predecessore è il Californio, l'elemento successivo è il Fermio. Il suo analogo nella serie dei lantanidi è l' olmio .
Proprietà fisiche
L'einsteinio è un metallo radioattivo con un punto di fusione di 860 ° C, un punto di ebollizione di 996 ° C e una densità di 8,84 g / cm 3 . Cristallizza nel sistema cristallino cubico nel gruppo spaziale Fm 3 m (gruppo spaziale n. 225) con il parametro reticolare a = 575 pm, che corrisponde a un reticolo cubico a facce centrate (fcc) o a un impaccamento cubico più vicino di sfere con la sequenza di impilamento ABC. La radioattività è così forte che distrugge la griglia metallica. Il metallo è bivalente e ha una volatilità notevolmente elevata.
Proprietà chimiche
Come tutti gli attinidi, l'Einsteinio è molto reattivo. Lo stato di ossidazione trivalente è più stabile in soluzione acquosa , ma sono noti anche composti bivalenti e tetravalenti. I composti bivalenti potrebbero già essere rappresentati come solidi; lo stato tetravalente potrebbe già essere postulato durante il trasporto chimico in quantità traccianti, ma si attende ancora una conferma definitiva. Le soluzioni acquose con ioni Es 3+ sono di colore rosa pallido.
istruzioni di sicurezza
Le classificazioni secondo il regolamento CLP non sono disponibili perché includono solo il rischio chimico e svolgono un ruolo del tutto subordinato rispetto ai pericoli basati sulla radioattività . Quest'ultimo si applica anche solo se la quantità di sostanza coinvolta è rilevante.
uso
L'einsteinio è utilizzato principalmente nella produzione di elementi transuranici superiori e transactinidi . Altrimenti, il metallo e i suoi composti vengono estratti principalmente in piccole quantità per scopi di studio.
link
→ Categoria: connessione Einsteinium
Lo studio dei composti dell'einsteinio è limitato da diversi fattori:
- L'isotopo più facilmente disponibile, 253, è disponibile solo una o due volte l'anno su una scala di microgrammi.
- Gli ordini a lungo raggio nei solidi vengono distrutti molto rapidamente dall'intensa radiazione alfa generata in un'emivita di circa 20 giorni .
- Il decadimento radioattivo produce gli isotopi 249 Bk e 249 Cf, che contaminano rapidamente il campione. Il tasso è di circa il 3% al giorno.
ossidi
L'ossido di Einsteinio (III) (Es 2 O 3 ) è stato ottenuto calcinando il corrispondente nitrato in quantità inferiori al microgrammo. Il parametro reticolare del cristallo cubico a corpo centrato è 1076,6 (6) pm . Sono anche note una struttura di ossido di lantanio (III) monoclina ed esagonale .
ossialogenuri
Sono noti gli ossialogenuri Einsteinio (III) ossicloruro (EsOCl), Einsteinio (III) ossibromuro (EsOBr) e Einsteinio (III) ossiioduro (EsOI). L'ossicloruro di Einsteinio (III) ha una struttura tetragonale del tipo PbFCl.
alogenuri
Gli alogenuri sono noti per i loro stati di ossidazione +2 e +3. Il livello più stabile +3 è noto per tutti i composti dal fluoro allo iodio ed è anche stabile in soluzione acquosa.
| Numero di ossidazione | f. | Cl | Br | IO. |
| +3 |
Fluoruro di Einsteinio (III) EsF 3 |
Einsteinio (III) cloruro EsCl 3 arancione |
Einsteinio (III) bromuro EsBr 3 bianco-giallo |
Einsteinio (III) ioduro EsI 3 color ambra |
| +2 |
Einsteinio (II) cloruro EsCl 2 |
Einsteinio (II) bromuro EsBr 2 |
Einsteinio (II) ioduro EsI 2 |
Il fluoruro di Einsteinio (III) (EsF 3 ) può essere preparato per precipitazione da soluzioni di cloruro di Einsteinio (III) con fluoruro, nonché da ossido di Einsteinio (III) per reazione con ClF 3 o F 2 a 1-2 atmosfere pressione e 300- 400°C. Non è stato possibile determinare la struttura cristallina, ma si presume che corrisponda al tipo LaF 3 , come per il fluoruro di Berkelio (III) (BkF 3 ) e il fluoruro di Californio (III) (CfF 3 ) .
Il cloruro di Einsteinio (III) (EsCl 3 ) è un solido di colore arancione e forma una struttura esagonale del tipo UCl 3 , l'atomo Es essendo coordinato 9 volte.
Il bromuro di Einsteinio (III) (EsBr 3 ) è un solido bianco-giallo e forma una struttura monoclina del tipo AlCl 3 .
Lo ioduro di Einsteinio (III) (EsI 3 ) è un solido di colore ambrato e forma una struttura esagonale di tipo BiI 3 .
I composti bivalenti dell'Einsteinio sono prodotti riducendo gli alogenuri trivalenti con l' idrogeno .
Per einsteinio (II) cloruro (EsCl 2 ), Einsteinio (II) bromuro (EsBr 2 ) e Einsteinio (II) ioduro (EsI 2 ), non sono noti dati cristallografici più dettagliati, ma sono noti i valori misurati delle bande di assorbimento.
letteratura
- Richard G. Haire: Einsteinium , in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (a cura di): The Chemistry of the Actinide and Transactinide Elements , Springer, Dordrecht 2006; ISBN 1-4020-3555-1 , pp. 1577-1620 ( doi: 10.1007 / 1-4020-3598-5_12 ).
- Glenn T. Seaborg (Ed.): Atti del Simposio per la Commemorazione del 25° Anniversario degli Elementi 99 e 100 , 23 gennaio 1978; Rapporto LBL-7701, aprile 1979.
- Gmelin's Handbook of Inorganic Chemistry , System No. 71, Transurane: Part A 1 II, pp. 20-21; Parte A 2, pp. 46-47; Parte B1, pp. 82-84.
- Caratterizzazione strutturale e spettroscopica di un complesso di Einsteinio
link internet
- Ingresso all'Einsteinium. In: Römpp Online . Georg Thieme Verlag, consultato il 3 gennaio 2015.
- Albert Ghiorso: Einsteinium and Fermium , Chemical & Engineering News, 2003.
- Nadja Podbregar: Nuova visione dell'elemento esotico Einsteinium , scinexx.de - 5 febbraio 2021
- L'elemento misterioso con 99 elettroni
Evidenze individuali
- ↑ I valori delle proprietà atomiche e fisiche (info box) sono, salvo diversa indicazione, tratti da: Richard G. Haire: Einsteinium , in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (ed.): La chimica degli elementi attinidi e transattinidi , Springer, Dordrecht 2006; ISBN 1-4020-3555-1 , pp. 1577-1620.
- ↑ a b c d e Entry on einsteinium in Kramide, A., Ralchenko, Yu., Reader, J. e NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1) . Ed.: NIST , Gaithersburg, MD. doi : 10.18434/T4W30F ( https://physics.nist.gov/asd ). Estratto il 13 giugno 2020.
- ↑ a b c d e entry on einsteinium at WebElements, https://www.webelements.com , consultato il 13 giugno 2020.
- ↑ I pericoli derivanti dalla radioattività non rientrano nelle proprietà da classificare secondo l'etichettatura GHS. Per quanto riguarda gli altri pericoli, questo elemento o non è stato ancora classificato o non è stata ancora trovata una fonte affidabile e citabile.
- ↑ a b c d e f g h i Albert Ghiorso: Einsteinium and Fermium , Chemical & Engineering News, 2003.
- ^ Albert Ghiorso , G. Bernard Rossi, Bernard G. Harvey, Stanley G. Thompson: Reactions of U 238 with Cyclotron-Produced Nitrogen Ions , in: Physical Review , 1954 , 93 (1), pp. 257-257 ( doi: 10.110 / PhysRev.93.257 ).
- ↑ SG Thompson, A. Ghiorso, BG Harvey, GR Choppin: Transcurium Isotopes Produced in the Neutron Irradiation of Plutonium , in: Physical Review , 1954 , 93 (4), pp. 908-908 ( doi: 10.1103/PhysRev.93.908 ) .
- ^ BG Harvey, SG Thompson, A. Ghiorso, GR Choppin: Ulteriore produzione di transcurio nuclidi per irradiazione di neutroni , in: Physical Review , 1954 , 93 (5), pp. 1129-1129 ( doi: 10.1103/PhysRev.93.1129 ).
- ↑ MH Studier, PR Fields, H. Diamond, JF Mech, AM Friedman, PA Sellers, G. Pyle, CM Stevens, LB Magnusson, JR Huizenga: Elements 99 and 100 from Pile-Irradiated Plutonium , in: Physical Review , 1954 , 93 (6), pp. 1428-1428 ( doi: 10.1103 / PhysRev.93.1428 ).
- ^ PR Fields, MH Studier, JF Mech, H. Diamond, AM Friedman, LB Magnusson, JR Huizenga: Additional Properties of Isotopes of Elements 99 and 100 , in: Physical Review , 1954 , 94 (1), pp. 209-210 ( doi: 10.1103 / PhysRev.94.209 ).
- ^ GR Choppin, SG Thompson, A. Ghiorso, BG Harvey: Nuclear Properties of Some Isotopes of Californium, Elements 99 and 100 , in: Physical Review , 1954 , 94 (4), pp. 1080-1081 ( doi: 10.1103/PhysRev .94.1080 ).
- ^ Hugo Atterling, Wilhelm Forsling, Lennart W. Holm, Lars Melander, Björn Åström: Element 100 Produced by Means of Cyclotron-Accelerated Oxygen Ions , in: Physical Review , 1954 , 95 (2), pp. 585-586 ( doi: 10.1103 / PhysRev.95.585.2 ).
- ^ GT Seaborg , SG Thompson, BG Harvey, GR Choppin: Chemical Properties of Elements 99 and 100 ( abstract ; machine script (23 luglio 1954), Radiation Laboratory, University of California, Berkeley, UCRL-2591 (Rev.) ).
- ^ SG Thompson, BG Harvey, GR Choppin, GT Seaborg: Proprietà chimiche degli elementi 99 e 100 , in: J. Am. Chimica Soc. , 1954 , 76 (24), pp. 6229-6236 ( doi: 10.1021/ja01653a004 ).
- ^ A b A. Ghiorso, SG Thompson, GH Higgins, GT Seaborg (Laboratorio di radiazioni e Dipartimento di chimica, Università della California, Berkeley, California) , MH Studier, PR Fields, SM Fried, H. Diamond, JF Mech, GL Pyle , JR Huizenga, A. Hirsch, WM Manning (Argonne National Laboratory, Lemont, Illinois) , CI Browne, HL Smith, RW Spence (Los Alamos Scientific Laboratory, Los Alamos, New Mexico) : Nuovi elementi Einsteinio e Fermio, Numeri atomici 99 e 100 , in: Physical Review , 1955 , 99 (3), pp. 1048-1049 ( doi: 10.1103 / PhysRev.99.1048 ; Maschinoscript (9 giugno 1955), Lawrence Berkeley National Laboratory. Paper UCRL-3036 ).
- ^ Campi di PR, MH Studier, H. Diamond, JF Mech, MG Inghram, GL Pyle, CM Stevens, S. Fried, WM Manning (Argonne National Laboratory, Lemont, Illinois) ; A. Ghiorso, SG Thompson, GH Higgins, GT Seaborg (University of California, Berkeley, California) : Transplutonium Elements in Thermonuclear Test Debris , in: Physical Review , 1956 , 102 (1), pp. 180-182 ( doi: 10.1103 /PhysRev.102.180 ).
- ^ A b Richard G. Haire: Einsteinium , in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (a cura di): The Chemistry of the Actinide and Transactinide Elements , Springer, Dordrecht 2006; ISBN 1-4020-3555-1 , pp. 1577-1620.
- ↑ G. Pfennig, H. Klewe-Nebenius, W. Seelmann-Eggebert (a cura di): Karlsruher Nuklidkarte , 7a edizione, 2006.
- ↑ Irshad Ahmad, Frank Wagner, Jr.: Emivita dell'isotopo di Einsteinio più longevo- 252 Es , in: J. Inorg. Nucl. Chem. , 1977 , 39 (9), pp. 1509-1511 ( doi: 10.1016 / 0022-1902 (77) 80089-4 ).
- ^ William McHarris, FS Stephens, F. Asaro, I. Perlman: Decay scheme of einsteinium-254 , in: Physical Review , 1966 , 144 (3), pp 1031-1045 ( doi: 10.1103 / PhysRev.144.1031 ).
- ^ G. Audi, O. Bersillon, J. Blachot, AH Wapstra: La valutazione NUBASE delle proprietà nucleari e di decadimento , in: Nuclear Physics A , 729, 2003, pp. 3-128. doi : 10.1016 / j.nuclphysa.2003.11.001 . ( PDF ; 1.0MB).
- ^ Reattore dell'isotopo ad alto flusso , laboratorio nazionale di Oak Ridge; Estratto il 23 settembre 2010.
- ^ Darleane C. Hoffman, Albert Ghiorso, Glenn Theodore Seaborg: The Transuranium People: The Inside Story , Imperial College Press, 2000, ISBN 978-1-86094-087-3 , pp. 190–191 ( anteprima limitata in Google Ricerca libri ).
- ^ M. Jones, RP Schuman, JP Butler, G. Cowper, TA Eastwood, HG Jackson: Isotopes of Einsteinium and Fermium Produced by Neutron Irradiation of Plutonium , in: Physical Review , 1956 , 102 (1), pp. 203-207 ( doi: 10.1103 / PhysRev.102.203 ).
- ^ LI Guseva, KV Filippova, Yu. B. Gerlit, VA Druin, BF Myasoedov, NI Tarantin: Experiments on the Production of Einsteinium and Fermium with a Cyclotron , in: Journal of Nuclear Energy , 1954 , 3 (4), pp. 341-346 (tradotto nel novembre 1956) ( doi: 10.1016 / 0891-3919 (56) 90064-X ).
- ^ A. Chetham-Strode, LW Holm: New Isotope Einsteinium-248 , in: Physical Review , 1956 , 104 (5), pp. 1314-1314 ( doi: 10.1103 / PhysRev.104.1314 ).
- ^ Bernard G. Harvey, Alfred Chetham-Strode, Albert Ghiorso, Gregory R. Choppin, Stanley G. Thompson: New Isotopes of Einsteinium , in: Physical Review , 1956 , 104 (5), pp. 1315-1319 ( doi: 10.1103 /PhysRev.104.1315 ).
- ^ SA Kulyukhin, LN Auerman, VL Novichenko, NB Mikheev, IA Rumer, AN Kamenskaya, LA Goncharov, AI Smirnov: Production of Microgram Quantities of Einsteinium-253 by the Reactor Irradiation of Californium , in: Inorganica Chimica Acta , 1985 , 110 ( 1), pp. 25-26 ( doi: 10.1016 / S0020-1693 (00) 81347-X ).
- ^ BB Cunningham, TC Parsons, USAEC Doc. UCRL-20426 (1971), pagina 239.
- ↑ a b R. G. Haire, RD Baybarz: Studies of einsteinium metal , in: Journal de Physique Colloques , 1979 , 40 (C4), pp. 101-102 ( doi: 10.1051/jphyscol: 1979431 ; PDF ; PDF ( machine script ) ) .
- ^ RG Haire: Properties of the Transplutonium Metals (Am-Fm) , in: Metals Handbook, Vol. 2, 10th Edition, (ASM International, Materials Park, Ohio, 1990), pp. 1198-1201.
- ^ Phillip D. Kleinschmidt, John W. Ward, George M. Matlack, Richard G. Haire: studi sulla vaporizzazione della legge di Henry e termodinamica dell'einsteinio - 253 metallo disciolto nell'itterbio , in: J. Chem. Phys. , 1984 , 81 , pp. 473-477 ( doi: 10.1063 / 1.447328 ).
- ^ AF Holleman , E. Wiberg , N. Wiberg : Manuale di chimica inorganica . 102a edizione. Walter de Gruyter, Berlino 2007, ISBN 978-3-11-017770-1 , p. 1956.
- ↑ a b D. D. Ensor, JR Peterson, RG Haire, JP Young: Studio spettrofotometrico di assorbimento di 253 EsF 3 e dei suoi prodotti di decadimento allo stato solido in fase bulk , in: J. Inorg. Nucl. Chem. , 1981 , 43 (10), pp. 2425-2427 ( doi: 10.1016 / 0022-1902 (81) 80274-6 ).
- ^ A b R. G. Haire, RD Baybarz: Identificazione e analisi del sesquiossido di Einsteinio mediante diffrazione elettronica , in: J. Inorg. Nucl. Chem. , 1973 , 35 (2), pp. 489-496 ( doi: 10.1016 / 0022-1902 (73) 80561-5 ).
- ↑ RG Haire, L. Eyring, in: Handbook on the Physics and Chemistry of Rare Earths , vol. 18 Lanthanoids and Actinides Chemistry (a cura di KA Gscheidner, Jr., L. Eyring, GR Choppin, GH Lander), North-Holland, New York 1994, pp. 414-505.
- ↑ a b c d e J. P. Young, RG Haire, JR Peterson, DD Ensor, RL Fellow: conseguenze chimiche del decadimento radioattivo. 2. Studio spettrofotometrico della crescita del berkelio-249 e del californio-249 negli alogenuri di Einsteinio-253 , in: Inorg. Chem. , 1981 , 20 (11), pp. 3979-3983 ( doi: 10.1021/ic50225a076 ).
- ↑ a b J. R. Peterson, DD Ensor, RL Fellows, RG Haire, JP Young: Preparazione, caratterizzazione e decadimento dell'einsteinio (II) allo stato solido , in: Journal de Physique Colloques , 1979 , 40 (C4), p. 111-113 ( doi: 10.1051/jphyscol: 1979435 ; PDF ).
- ^ AF Holleman , E. Wiberg , N. Wiberg : Manuale di chimica inorganica . 102a edizione. Walter de Gruyter, Berlino 2007, ISBN 978-3-11-017770-1 , p. 1969.
- ^ JP Young, RG Haire, RL Fellows, JR Peterson: Studi spettrofotometrici di alogenuri e ossialogenuri di elementi transcuriali allo stato solido , in: Journal of Radioanalytical Chemistry , 1978 , 43 (2), pp. 479-488 ( doi: 10.1007/ BF02519508 ).
- ↑ DK Fujita, BB Cunningham, TC Parsons, JR Peterson: Lo spettro di assorbimento in soluzione di Es 3+ , in: Inorg. Nucl. Lett. Chim. , 1969 , 5 (4), pp. 245-250 ( doi: 10.1016 / 0020-1650 (69) 80192-3 ).
- ↑ DK Fujita, BB Cunningham, TC Parsons: Strutture cristalline e parametri reticolari del tricloruro di einsteinio e dell'ossicloruro di einsteinio , in: Inorg. Nucl. Lett. Chim. , 1969 , 5 (4), pp. 307-313 ( doi: 10.1016 / 0020-1650 (69) 80203-5 ).
- ^ RL Fellows, JR Peterson, M. Noé, JP Young, RG Haire: diffrazione dei raggi X e studi spettroscopici del bromuro di einsteinio cristallino (III), 253 EsBr 3 , in: Inorg. Nucl. Lett. Chim. , 1975 , 11 (11), pp. 737-742 ( doi: 10.1016 / 0020-1650 (75) 80090-0 ).
- ^ RG Haire, Rapporto ORNL 5485, 1978 .
- ^ JR Peterson: Proprietà chimiche dell'Einsteinio: Parte II , in: GT Seaborg (Ed.): Atti del 'Simposio commemorativo del 25° anniversario degli elementi 99 e 100' , 23 gennaio 1978; Rapporto LBL-7701, aprile 1979, pp. 55-64.
- ^ RL Fellows, JP Young, RG Haire, JR Peterson, in: The Rare Earths in Modern Science and Technology (a cura di GJ McCarthy e JJ Rhyne), Plenum Press, New York 1977, pp. 493-499.
- ^ JP Young, RG Haire, RL Fellows, M. Noé, JR Peterson: Spectroscopic and X-ray Diffraction Studies of the Bromuri of Cf-249 and Es-253 , in: Transplutonium 1975 (a cura di W. Müller e R. Lindner ), Olanda Settentrionale, Amsterdam 1976, pp. 227-234.

![\ mathrm {^ {238} _ {\ 92} U \ {\ xrightarrow [{- 2 \ \ beta ^ {-}}] {+ \ 6 \ (n, \ gamma)}} \ _ {\ 94} ^ {244} Pooh}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c4b60ac4bf0d4ebf96b6a71fefa86f13dd5784e0)
![\ mathrm {^ {238} _ {\ 92} U \ {\ xrightarrow [{- 7 \ \ beta ^ {-}}] {+ \ 15, \ 16, \ 17 \ (n, \ gamma)}} \ _ {\ \ \ \ \ \ \ \ \ \ \ \ 99} ^ {253, \ 254, \ 255} Es}](https://wikimedia.org/api/rest_v1/media/math/render/svg/40a621970bb60c515339d427edbe5018ca880d2c)
![\ mathrm {^ {252} _ {\ 98} Cf \ {\ xrightarrow {(n, \ gamma)}} \ _ {\ 98} ^ {253} Cf \ {\ xrightarrow [{17,81 \ d}] {\ beta ^ {-}}} \ _ {\ 99} ^ {253} It \ {\ xrightarrow {(n, \ gamma)}} \ _ {\ 99} ^ {254} It \ {\ xrightarrow [{ }] {\ beta ^ {-}}} \ _ {100} ^ {254} Fm}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2dcf5875c42aad904ed8c8a397de8fc552cf5f71)
![\ mathrm {^ {249} _ {\ 98} Cf \ + \ _ {1} ^ {2} D \ \ longrightarrow \ _ {\ 99} ^ {248} Es \ + \ 3 \ _ {0} ^ { 1} n \ quad \ sinistra (^ {248} _ {\ 99} Es \ {\ xrightarrow [{27 \ min}] {\ epsilon}} \ _ {\ 98} ^ {248} Cf \ destra)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/85115ad812c3c66ccfd6c7741439fce1fc1be1c2)
![\ mathrm {^ {249} _ {\ 97} Bk \ {\ xrightarrow [{- \ 4 \ a \ 1 \ n}] {+ \ alpha}} \ _ {\ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ 99} ^ {249, \ 250, \ 251, \ 252} Es}](https://wikimedia.org/api/rest_v1/media/math/render/svg/16e216c81a272463e710f8aa9d0f10f819a0589c)
![\ mathrm {^ {252} _ {\ 98} Cf \ {\ xrightarrow {(n, \ gamma)}} \ _ {\ 98} ^ {253} Cf \ {\ xrightarrow [{17,81 \ d}] {\ beta ^ {-}}} \ _ {\ 99} ^ {253} Es}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5f409bd2bd31e6e316748643fc25eb44d318bef5)



![\ mathrm {^ {253} _ {\ 99} Es \ {\ xrightarrow [{20 \ d}] {\ alpha}} \ _ {\ 97} ^ {249} Bk \ {\ xrightarrow [{314 \ d} ] {\ beta ^ {-}}} \ _ {\ 98} ^ {249} Cf}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a2e6d53c027c0247a7ddbc0c45718d09789f2da2)

